1.8.1 Faradayův zákon – vylučování kovů
Pro získávání elektrolytické mědi z měďnaté soli byl navržen elektrolyzér pracující s proudem 1560 A s účinností 85 %. Vypočítejte výkon elektrolyzéru (v kg kovu za hodinu). Molární hmotnost mědi je 63,55 g mol−1.
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek
1,572 kg mědi za hodinu
Postup
Přímá aplikace Faradayova zákona. Pozor na převod jednotek!
Audio
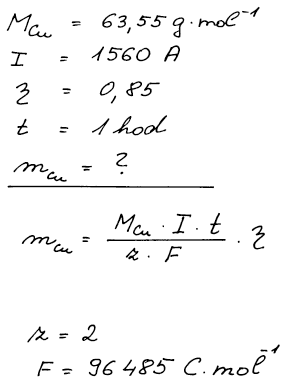
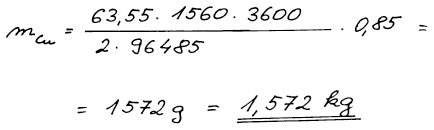
Při výpočtu vycházíme z Faradayova zákona, kde z je počet elektronů,
které ion ztrácí nebo získává během elektrolýzy. V tomto případě se
měďnatý ion redukuje na kovovou měď a získává 2 elektrony.
Při dosazování do rovnice pro výpočet hmotnosti je třeba dosazovat
všechny údaje v základních jednotkách SI, to znamená čas v sekundách.