3.4.2 Výpočet reakční entalpie na základě slučovacích entalpií látek
Vypočítejte teplo, které se za teploty 25 °C uvolní při izobarické přeměně 1 kg pyritové rudy na Fe2O3 a SO2 za konstantního tlaku. Výchozí surovina obsahuje 70 % pyritu (FeS2).
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek
ΔH° = −3339,34 kJ/ mol Q = 4869,6 kJ
Řešení
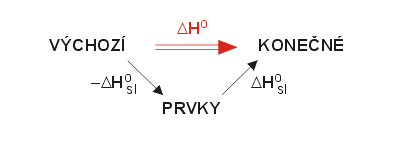
Přeměna probíhá podle reakce
![]()
Reakční teplo určíme podle vztahu (3.22)
![]()
na základě slučovacích tepel, která nalezneme v tabulkách.
![]()
Při přeměně 4 mol FeS2, tj. 4 . 119,97 = 479,90 g FeS2, přejde do okolí 3339,34 kJ. Z 1000 g 70 %-ní rudy, tj. ze 700 g FeS2, získáme 3339,34 . 700/479,90 = 4870,9 kJ.