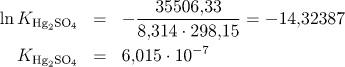7.2.19 Výpočet součinu rozpustnosti ze standardních elektrodových potenciálů
Pomocí hodnot standardních elektrodových potenciálů, uvedených v tabulkách vypočítejte součin rozpustnosti síranu rtuťného při teplotě 25 °C.
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek
KHg2SO4 = 6,015.10−7
Řešení
Disociace síranu rtuťného probíhá podle rovnice
![]()
Součin rozpustnosti síranu rtuťného je dán vztahem
![]()
Tato rovnice definuje rovnovážnou konstantu disociace. Tuhý síran rtuťný je ve svém standardním stavu a jeho aktivita je proto jednotková. Pro součin rozpustnosti tedy platí
![]()
kde ΔG° je změna standardní Gibbsovy energie reakce. Reakci lze získat kombinací reakcí odpovídajících redukčním reakcím na kalomelové a rtuťové elektrodě, tj.
![]()
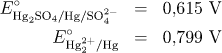
Reakce je rozdílem dílčích pochodů (1) a (2) a pro změnu standardní Gibbsovy energie reakce tedy platí vztah (7.20)
![]()
Součin rozpustnosti síranu rtuťného
získáme po dosazení
do uvedené rovnice: