6.1.48 Simultánní reakce
Vypočítejte složení rovnovážné plynné směsi při izomeraci hexanu za teploty 400 K a atmosférického tlaku. Předpokládejte, že se všechny složky chovají jako ideální plyny a že na počátku obsahuje reakční směs pouze plynný hexan. Potřebné údaje vyhledejte v tabulkách .
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek

Postup
V tabulkách nalezneme hodnoty slučovacích Gibbsových energií jednotlivých komponent a vypočteme hodnoty změn standardních Gibbsových energií jednotlivých reakcí

Ze vztahu (6.7) vypočteme rovnovážné konstanty těchto reakcí a vyjádříme jednotlivé reakční rozsahy:
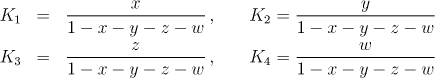
Nyní vyjádříme rozsahy reakce y, z a w s použitím rozsahu reakce x:
![]()
Dosazením těchto vztahů do rovnice pro rovnovážnou konstantu K1 a úpravou vypočítáme rozsah reakce x:
![]()
Hodnoty ostatních rozsahů reakce určíme zpětným výpočtem.
Řešení
V soustavě mohou zároveň probíhat čtyři nezávislé reakce:

Jakékoli další přechody mezi jednotlivými izomery hexanu lze vyjádřit jako kombinaci těchto čtyř reakcí. Pro slučovací Gibbsovy energie jednotlivých izomerů hexanu při teplotě 400 K lze v tabulkách nalézt tyto hodnoty (v kJ/mol):

![]()
Hodnoty rovnovážných konstant vypočítáme ze vztahu (6.7) a po dosazení postupně získáme rovnice
![]()
Nyní sestavíme látkovou bilanci systému. Jako základ výpočtu zvolíme jeden mol hexanu. Protože v soustavě probíhají zároveň čtyři nezávislé reakce, musíme zavést čtyři rozsahy reakce :

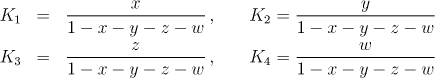
Nyní vyjádříme rozsahy reakce y, z a w s použitím rozsahu reakce x:
![]()
Dosazením těchto vztahů do rovnice pro rovnovážnou konstantu K1 a úpravou vypočítáme rozsah reakce x:
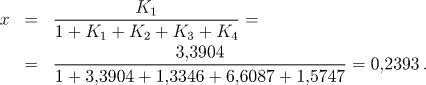
Hodnoty ostatních rozsahů reakce určíme zpětným výpočtem:
![]()
Z těchto hodnot vypočítáme složení rovnovážné směsi:
