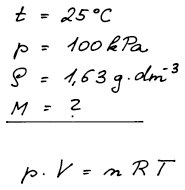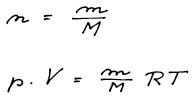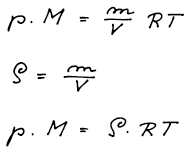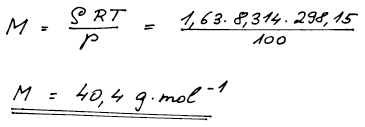1.2.2 Jaký plyn izoloval Ramsay?
W. Ramsay získal ze vzduchu po několikanásobné adsorpci na aktivním uhlí malé množství plynu, u kterého při teplotě 25 °C a tlaku 100 kPa určil hustotu ϱ = 1,63 g dm−3. Jakou hodnotu molární hmotnosti plynu dostal Ramsay výpočtem ze stavové rovnice ideálního plynu? Jaký plyn to byl?
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓