6.1.32 Reakce páry s tuhou látkou
Vodní pára reaguje se žhavým koksem podle rovnice
![]()
Rovnovážná konstanta této reakce má při teplotě 1000 K hodnotu 2,609; pro plynné složky je použit standardní stav f° = 101,325 kPa a pro C(s) čistá složka za teploty a tlaku soustavy. Vypočítejte, kolik tun vodní páry se spotřebuje na zreagování jedné tuny koksu za uvedené teploty a tlaku 97 kPa. Předpokládejte ideální chování plynů.
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek
Na úplné zreagování 1 t koksu spotřebujeme 1,754 t vodní páry.
Postup
Z látkové bilance, ve které neuvažujeme uhlík (není v plynné směsi, jeho aktivita je jednotková):

![]()
Pozor: ∑i νi se počítá také bez stechiometrického koeficientu tuhé složky!! Nyní spočteme počet molů uhlíku ξ zreagovaných na 1 mol vstupující vodní páry a jednoduchou úměrou:
![]()
vypočteme množství tun vodní páry na 1 t koksu.
Řešení
Tuhá složka reakce (chemické individuum) je při tomto typu reakcí ve standardním stavu, a proto je její aktivita rovna jedné. Do látkové bilance pro dosazení do rovnovážné konstanty se tedy zahrnují pouze plynné složky. U reakcí, při kterých se zahříváním tuhé složky uvolňují plynné produkty se často počítá tzv. rozkladná teplota, tedy teplota, při níž se tlak par vznikajících plynných složek vyrovná s tlakem atmosferickým a tuhá složka se rozkládá.
Pro rovnovážnou konstantu reakce platí vztah
![]()
Tuhý uhlík je ve standardním stavu, a proto je jeho aktivita rovna jedné. Do látkové bilance tedy zahrneme pouze plynné složky. Jako základ výpočtu zvolíme 1 mol vodní páry a bilanci uspořádáme do tabulky:

![]()
Po úpravě vypočítáme rozsah reakce
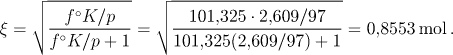
Z jednotkového látkového množství vodní páry, vstupujícího do reaktoru, zreaguje 0,8553 mol, stejné množství zreaguje i uhlíku (viz stechiometrii reakce). Na přeměnu 0,8553 mol uhlíku tedy spotřebujeme 1 mol vodní páry. Množství páry, potřebné na 1 t koksu, vypočítáme úměrou
![]()
Na úplné zreagování 1 t koksu spotřebujeme 1,754 t vodní páry.