2.21 Směšování kapalin 
Směšování vody a kyseliny sírové je silně exotermické. Z toho plyne:
a) tyto dvě látky netvoří ideální směs
b) entalpie systému obsahující směs látek po smíšení je
(při stejné teplotě a tlaku a stejných množství) větší než
entalpie čisté vody a kyseliny sírové
c) dodatková entalpie HE < 0
d) dodatková entalpie HE > 0
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek
a) tyto dvě látky netvoří ideální směs
c) dodatková entalpie HE < 0
Řešení
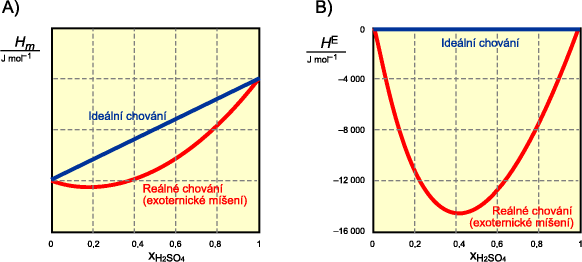
Na obrázku A) je uvedena závislost entalpie na složení u dvousložkové směsi pro ideální systém a pro
systém s exotermickým míšením. Na obrázku B) jsou uvedeny korespondující závislosti dodatkové entalpie.
Kdyby se kyselina sírová a voda tvořily ideální směs, nepozorovali bychom při míšení žádný tepelný
efekt; platí tedy varianta a).
Exotermický děj znamená, že systém teplo odevzdává do okolí (Q < 0); za
konstantní teploty a tlaku tedy entalpie klesá (varianta b) neplatí).
Při směšování tomuto ději odpovídají záporné hodnoty dodatkové entalpie
(HE < 0) – varianta c).