10.6.3 Rovnováha kapalina–kapalina – titrace
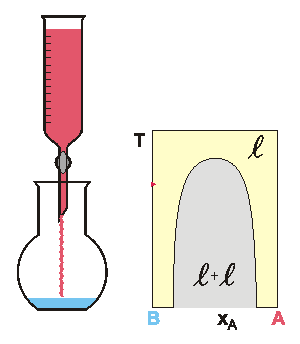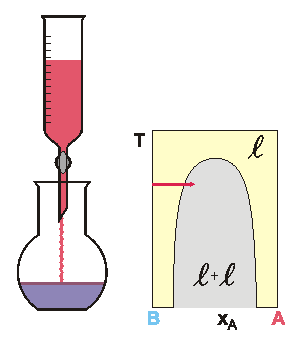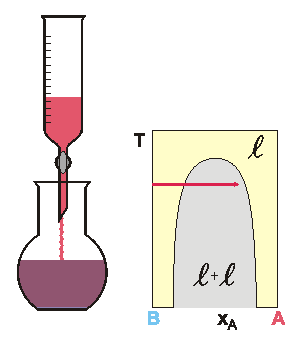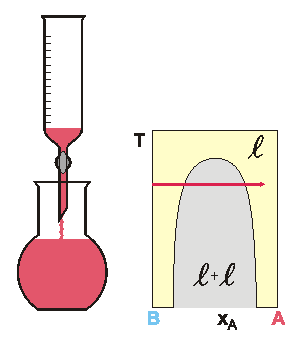 Koexistující kapalné fáze v systému voda(1) + 1-butanol(2) mají
při 25 °C složení vyjádřené molárním zlomkem vody
Koexistující kapalné fáze v systému voda(1) + 1-butanol(2) mají
při 25 °C složení vyjádřené molárním zlomkem vody ![]() a
a ![]() . Zjistěte, zda v systému
vzniknou dvě kapalné fáze, jestliže smícháme 100 g vody a 100 g
1-butanolu. Pokud ano, určete jejich látkové množství a hmotnost
vody (v g), kterou musíme přidat, aby vymizela butanolová fáze.
(Mbutanol = 74,08 g mol−1).
. Zjistěte, zda v systému
vzniknou dvě kapalné fáze, jestliže smícháme 100 g vody a 100 g
1-butanolu. Pokud ano, určete jejich látkové množství a hmotnost
vody (v g), kterou musíme přidat, aby vymizela butanolová fáze.
(Mbutanol = 74,08 g mol−1).
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek
V systému se vytvoří 2 fáze. nvod.f. = 4,307 mol, nbut.f. = 2,593 mol, m = 1155,6 g vody.
Postup
Provedeme látkovou bilanci obou složek za použití vztahu
![]()
kde index i označuje složku a pruhy nad symboly odlišují obě fáze.
Látková množství obou látek určíme z jejich hmotností podle n = m/M.
Tuto soustavu vyřešíme pro neznámé ![]() a
a ![]() .
Pokud obě látková množství budou kladná, rozpadne se systém
do dvou fází.
.
Pokud obě látková množství budou kladná, rozpadne se systém
do dvou fází.
Látkové množství vody v okamžiku vymizení butanolové fáze
určíme při znalostí látkového množství butanolu ze vztahu
![]()
Hmotnost přidané vody pak vypočteme jako rozdíl odpovídající celkové hmotnosti vody a její hmotnosti na počátku.