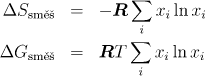4.2.14 Směšovací entropie a Gibbsova energie
Vypočtěte změnu molární entropie a změnu molární Gibbsovy energie při smísení benzenu a toluenu. Vzniklá směsi obsahuje 30 mol.% benzenu. Směšování probíhá při 25 °C a směs se chová jako ideální roztok.
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓