3.1.1 Výpočet Q, W, ΔU za konstantního tlaku ze závislosti tepelné kapacity na teplotě
Molární tepelnou kapacitu (v J mol−1 K−1) vodní páry ve stavu ideálního plynu vystihuje v teplotním intervalu 300 až 1000 K vztah
![]()
S pomocí tohoto vztahu vypočítejte:
a) teplo Q, objemovou práci W, změnu vnitřní energie ΔU a změnu entalpie ΔH doprovázející ohřátí 1 mol páry za
tlaku 100 kPa z teploty 400 K na teplotu 600 K,
b) střední molární tepelnou kapacitu vodní páry pro teplotu 300
až 400 K, 300 až 500 K, ..., 300 až 1000 K,
c) na základě
vypočítaných středních tepelných kapacit určete teplo potřebné
na ohřátí 1 mol vodní páry z 400 K na 600 K.
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek
a) Q = 7067,2 J ΔU = 5404,4 J W = −1662,8 J
| T/K | 300 | 400 | 500 | 600 | 700 | 800 | 900 | 1000 |
|
| 33,57 | 33,98 | 34,41 | 34,88 | 35,38 | 35,91 | 36,47 | 37,06 |
Řešení
a) Protože jde o izobarický děj, platí
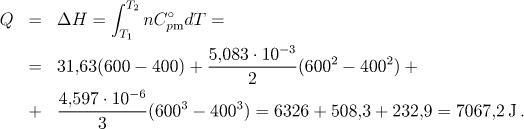
Změnu vnitřní energie vodní páry určíme podle rovnice
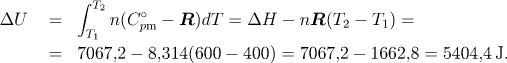
Práce při izobarickém ději je dána vztahem
![]()
b) Střední tepelná kapacita je definována vztahem
![]()
S použitím uvedené závislosti pro molární tepelnou kapacitu získáme
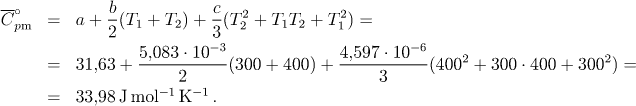
Ostatní hodnoty ![]() uvádíme v tabulce:
uvádíme v tabulce:
| T/K | 300 | 400 | 500 | 600 | 700 | 800 | 900 | 1000 |
|
| 33,57 | 33,98 | 34,41 | 34,88 | 35,38 | 35,91 | 36,47 | 37,06 |
c) Podle definiční rovnice pro ![]() můžeme
psát
můžeme
psát
![]()
Požadované teplo určíme ze vztahu
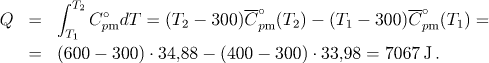
(Malý rozdíl proti výsledku v bodu a) vznikl zaokrouhlením ![]() na dvě desetinná místa.)
na dvě desetinná místa.)