4.2.11 Změna termodynamických funkcí při smíšení ideálních plynů
Vypočítejte změnu termodynamických funkcí U, H, S, G, F, která odpovídá smíšení 1 m3 dusíku se 4 m3 kyslíku při t = 0 °C a p = 0,1 MPa. Oba plyny považujte za ideální.
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek
[nN2 = 44,03 mol nO2 = 176,14 mol xN2 = 0,20 xO2 = 0,80]
![]() = 915,94 J/K
= 915,94 J/K
![]() = −250188 J
= −250188 J
![]() = 250188 J
= 250188 J
![]()
Řešení
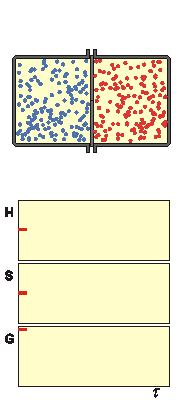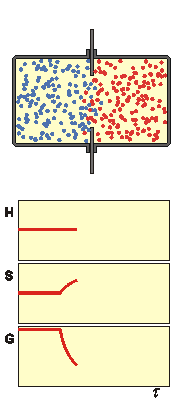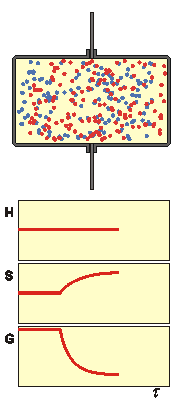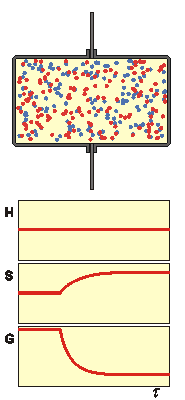
Směšovací entropie je definována rovnicí (4.18)
![]()
Látková množství vypočítáme ze stavové rovnice ideálního plynu:
![]()
![]()
a pro molární zlomky platí
![]()
Tyto údaje dosadíme do vztahu pro směšovací entropii:
![]()
Protože je teplota konstantní, pro ideální plyny platí
![]()
Směšovací Gibbsovu energii určíme z rovnice (4.19)
![]()
Pro směšovací Helmholtzovu energie platí
![]()