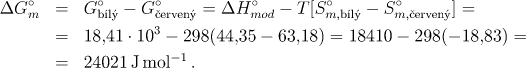4.2.7 Změna Gibbsovy energie při fázové přeměně
Při studiu anorganické chemie jste se dověděli, že existuje
několik alotropických modifikací fosforu, z nichž je nejznámější
červený a bílý fosfor. Na základě termodynamického výpočtu
zjistěte, která z těchto modifikací je stálejší při 25 °C.
K dispozici máte hodnoty absolutní entropie červeného fosforu
S°m = 63,18 J mol−1 K−1a bílého fosforu S°m = 44,35 J mol−1 K−1, dále
pak i entalpii modifikační přeměny
P(červený, 25 °C) →
P(bílý, 25 °C), ΔH°mod = 18,41 kJ/mol.
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek
ΔG°m = 24021 J/mol
Z výpočtu je zřejmé, že nižší hodnotu Gibbsovy energie vykazuje červená
modifikace, která je tedy za daných podmínek stálejší.
Řešení
Větší stálost bude vykazovat modifikace s nižší hodnotou Gibbsovy energie, neboť chemické reakce mají tendenci probíhat za konstantní teploty a tlaku do rovnovážného (stabilního) stavu, v němž je hodnota Gibbsovy energie nejnižší.
Při řešení vycházíme z rovnice