6.1.35 Reakce v plynné fázi s tuhou složkou III
Dusík v tlakové láhvi je znečištěn příměsí kyslíku, který chceme odstranit vedením dusíku aparaturou, obsahující rozžhavenou měď. V aparatuře je atmosférický tlak a teplota 1200 K. Vypočítejte zbytkový tlak kyslíku v aparatuře za předpokladu, že se v ní ustaví dokonalá rovnováha. Reakce
![]()
má při teplotě 1200 K standardní změnu Gibbsovy energie −82,19 kJ/mol.
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek
pO2 = 0,00708 Pa.
Postup
![]()
Pro ideální chování plynné složky platí ai = pi/fi°, aktivita tuhé složky je jednotková (je ve svém standardním stavu). Pro rovnovážnou konstantu lze zapsat:
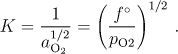
Pozor Δν je rovno −0,5, neboť na aktivitě v plynné fázi se podílí pouze plynná složka a tudíž se nepočítá se stechiometrickými koeficienty tuhých složek !! Ze zadáné hodnoty standardní změny Gibbsovy energie spočteme rovnovážnou konstantu pomocí vztahu (6.7)
![]()
a odtud určíme rovnovážný tlak pO2.