1.23 Elektrolýza 
Do oddělení, které provozuje elektrolýzu NaCl a získaný Na převádí na NaOH (MNaOH = 40 g mol−1), přišla zakázka na výrobu 40 kg NaOH a 40 kg kapalného chlóru (MCl2 = 71 g mol−1). Jaký elektrický náboj musí minimálně projít elektrolyzérem? Faradayova konstanta je F = 96500 C mol−1.
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek
Bude třeba náboj Q = 1,1 . 103F = 106150 . 103 C.
Řešení
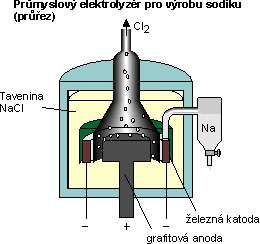 Pro výrobu sodíku se provádí elektrolýza taveniny NaCl. Celková reakce tohoto děje je
Pro výrobu sodíku se provádí elektrolýza taveniny NaCl. Celková reakce tohoto děje je
![]()
Při reakci kovového sodíku s vodou pak vzniká NaOH a vodík podle reakce
![]()
Pro správné řešení úlohy je třeba rozhodnout, jestli je potřeba více náboje na výrobu 40 kg sodíku, nebo na výrobu 40 kg chlóru.
Můžeme postupovat dle úvahy
| na výrobu 1 mol | .... 40 g NaOH | ...... 1 . F náboje |
| na výrobu | .... 40 kg NaOH | ...... 1000 . F náboje |
| na výrobu 1/2 mol | .... 35,5 g Cl2 | ...... 1 . F náboje |
| na výrobu | .... 40 kg Cl2 | ...... |
Na výrobu 40 kg chlóru je třeba více náboje než na výrobu stejné hmotnosti sodíku. Je nutno dodat 1,1 . 103F = 106150 . 103 C. Vyrobí se tudíž více sodíku než je třeba.