1.1.13 Stanovení molární hmotnosti metodou limitních hustot
V literatuře jsou uvedeny následující hodnoty měrného objemu par methanolu v závislosti na tlaku platné pro teplotu 100 °C.
| p/(kPa) | 50 | 100 | 150 |
| Vsp/(cm3/g) | 1,912 | 0,9435 | 0,6203 |
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek
M = 32,05 g/mol.
Postup
![]()
Řešení
Zdánlivou molární hmotnost určíme ze stavové rovnice ideálního plynu (zdánlivá je tato molární hmotnost proto, že stavová rovnice ideálního plynu platí exaktně jen při nulovém tlaku, skutečná molární hmotnost není závislá na tlaku)
![]()
Pro p = 50 kPa získáme
![]()
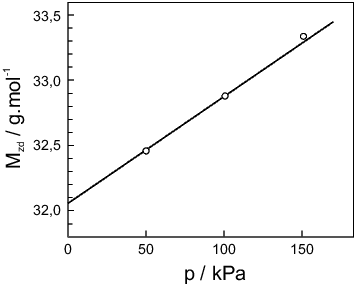
Pro p = 100 kPa dostaneme Mzd = 32,88 a pro p = 150 kPa Mzd = 33,34 g/mol. Skutečnou hodnotu molární hmotnosti určíme ze vztahu
![]()
např. grafickou metodou. Ze závislosti Mzd na p uvedené na obrázku získáme tímto způsobem hodnotu M = 32,05 g/mol.