8.5.19 Kombinace následné a vratné reakce
Nakreslete schematicky průběh koncentrací látek A, B a C v závislosti na čase,
které reagují podle reakčního schematu
A![]() B
B ![]() C
C
Pro případ cA0 = 2 mol/dm3, k1 = 0,01 s−1,
k2 = 0,006 s−1, k3 = 0,002 s−1,
určete konečné koncentrace všech tří látek.
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
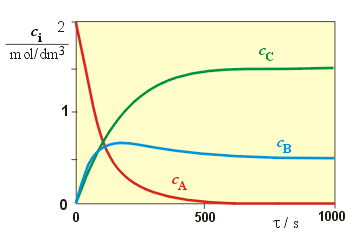 τ = ∞, cA = 0,cB = 0,5 mol/dm3, cC = 1,5 mol/dm3.
τ = ∞, cA = 0,cB = 0,5 mol/dm3, cC = 1,5 mol/dm3.