10.3.13 Závislost aktivitního koeficientu na složení a výpočet azeotropu
Na základě dále uvedených dat určete u směsi benzen(1)+cyklohexan(2):
a) složení parní fáze při x1 = 0,70 a t = 77,7 °C,
b) složení azeotropické směsi při teplotě 77,7 °C a tlak
v azeotropickém bodě.
Data: x1 = 0,40, y1 = 0,422, t = 77,7 °C, p = 101,32 kPa,
![]() = 94,1 kPa,
= 94,1 kPa,
![]() = 92,4 kPa.
= 92,4 kPa.
Předpokládejte, že uvažovaný systém se v kapalné fázi chová jako
regulární roztok, tj. platí relace
![]()
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek
x1,a = y1,a = 0,526, p = 101,8 kPa
Řešení
a) Na základě zadaného experimentálního údaje vypočítáme aktivitní koeficienty při x1 = 0,4 a z nich parametr b v rovnici (10.35). S použitím získaného parametru určíme aktivitní koeficienty při složení x1 = 0,70, tlak i složení parní fáze.
Aktivitní koeficienty určíme ze vztahu
![]()
Parametr b ve vztahu (10.35) bude mít hodnoty
![]()
Pro další výpočet použijeme hodnotu b = 0,35. Pro x1 = 0,7 dostaneme
![]()
Tlak a složení parní fáze určíme podle rovnic (10.36) a (10.37)
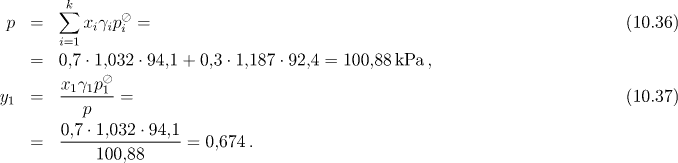
b) V azeotropickém bodě z podmínky yi = xi, i = 1,2 plyne
![]()
Po zlogaritmování dostaneme
![]()
Dosadíme-li za aktivitní koeficienty ze vztahu (10.35), bude platit
![]()
kde x1,az je hledané složení azeotropu. Z poslední rovnice pro x1,az dostaneme
![]()
Pro výpočet tlaku v azeotropickém bodě potřebujeme opět znát aktivitní koeficienty γi, které určíme z rovn. (10.35)
![]()
Po dosazení do rovnice (10.36) dostaneme hodnotu
![]()
V případě, že tlaky nasycených par složek jsou málo odlišné, může se azeotropický bod vyskytovat i u systémů, které mají malé odchylky od Raoultova zákona.