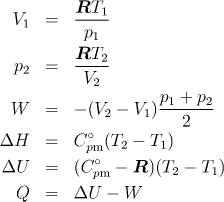3.2.8 Změny termodynamických veličin po přímce v p−V diagramu
Systém obsahující 1 mol ideálního plynu je převeden vratně ze
stavu (1) o parametrech T1=600 K, p1=300 kPa po přímce
v p−V diagramu do stavu (2). Vypočtěte příslušné změny
vnitřní energie, entalpie, teplo a práci, jestliže stavu (2)
přísluší parametry T2=1000 K,
Vm2=30 dm3/mol a molární tepelná kapacita plynu je
C°pm=32 J mol−1 K−1.
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek
[ Vm1 = 16,63 dm3/ mol, p2 = 277,1 kPa ] , W = −3859 J mol−1, ΔU = 9474,4 J mol−1, ΔH = 12800 J mol−1, Q = 13333 J mol−1.
Postup
Při ději po přímce v p−V diagramu se mění teplota, tlak i objem. Proto je nutné vypočítat teplo z práce a změny vnitřní energie. Použijte následující vztahy (viz řešený příklad 3.2.1):