3.6.1 Výpočet adiabatické teploty při spalování vodíku
Spalná entalpie vodíku [na H2O(g)] při 300 K má hodnotu
(ΔH°sp)H2 = −240 kJ/mol. Určete, jaké teploty
bude dosaženo při spalování H2 za adiabatických
podmínek teoretickým množstvím vzduchu (pro jednoduchost
předpokládejte, že vzduch obsahuje 20 mol. % kyslíku a zbytek je
dusík). Vodík i vzduch přicházejí do reaktoru s teplotou 300 K.
Předpokládejte, že spálení proběhne ze 100 % a při výpočtu
použijte tato data:
(C°pm)O2 = (C°pm)N2 = 34 J mol−1 K−1 , (C°pm)H2O = (28+0,012T) J mol−1 K−1 .
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek
![]()
Řešení
Při proběhnutí reakce za adiabatických podmínek se teplo, které by při izotermickém provedení přešlo do okolí, využije na ohřátí produktů (popř. i inertů). Dosažená teplota se označuje jako teplota adiabatická Tad. Je-li teplota výchozích látek rovna teplotě, při které známe reakční entalpii (tj. (Tvých = T1), platí vztah (3.28)
![]()
V našem případě (při spálení 1 mol H2 teoretickým množstvím vzduchu výše uvedeného složení) bude systém obsahovat:
| Látka | (ni)vých/ mol | (ni)kon/ mol |
| H2 | 1 | 0 |
| O2 | 0,5 | 0 |
| H2O | 0 | 1 |
| N2 | 2 | 2 |
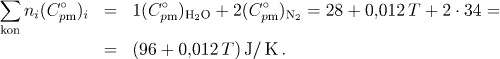
Dosazením do rovn.(3.28) a integrací dostaneme
![]()
Malou úpravou získáme kvadratickou rovnici
![]()
Z jejího řešení vyplývá Tad = 2435 K (druhý kořen je záporný a nemá fyzikální význam).