3.6.2 Entalpická bilance při konverzi SO2 na SO3
Plyny (ze sírové pece) o složení 8 mol. % SO2, 13 mol. %
O2 a 79 mol. % N2 slouží k výrobě SO3. V reaktoru
probíhá reakce (za konstantního tlaku)
SO2 + ![]() O2 = SO3 .
O2 = SO3 .
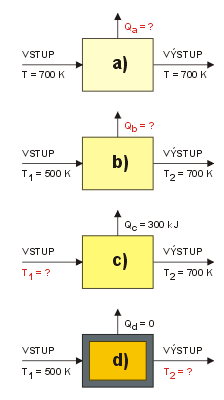
Vypočítejte tyto údaje (vypočítané hodnoty vztáhněte na 100 mol
výchozí směsi plynu a předpokládejte úplnou konverzi SO2 na SO3):
a) Teplo Qa potřebné k udržení ustáleného chodu reaktoru, do
nějž přicházejí plyny s teplotou Tvých = 700 K;
reakce má probíhat při teplotě 700 K a reakční zplodiny mají
odcházet
rovněž s teplotou 700 K.
b) Teplo Qb, potřebné pro reakci, jestliže produkty odchází
z reaktoru o teplotě 700 K a vstupní plyny mají teplotu 500 K.
c) Jaká je teplota vstupních plynů, jestliže se na 100 mol výchozí
směsi z reaktoru odvede 300 kJ tepla a teplota produktů je 700 K.
d) Konečnou teplotu Tad při adiabatickém proběhnutí reakce.
Plyny vstupující do reaktoru mají teplotu 500 K.
Při výpočtu použijte tato data (údaje pro oxid siřičitý a sírový nalezněte
v tabulkách):
![]()
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
Výsledek
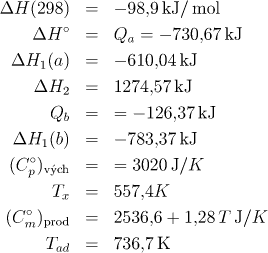
Řešení
a) Protože zreaguje 8 mol CO2, je podle definice reakčního tepla
při teplotě T teplo Qa za daných podmínek rovno osminásobku
reakčního tepla reakce při teplotě 700 K,
které můžeme určit podle Kirchhoffova zákona.
Proto použijeme vztah (viz řešený příklad 3.5.1)
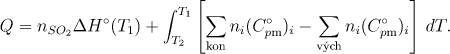
Reakční teplo při T1 = 298 K je rovno
![]()
Po dosazení do předchozího vztahu a integraci dostaneme
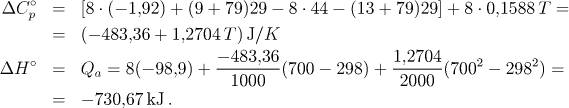
Z reaktoru musíme odebrat 730,7 kJ.
b) Reakce probíhá za stálého tlaku, a proto je teplo rovno změně
entalpie. Protože je entalpie stavová funkce, můžeme celkovou
změnu entalpie rozdělit do tří dílčích kroků. Platí tedy
![]()
Jednotlivé změny entalpie vypočítáme ze vztahů
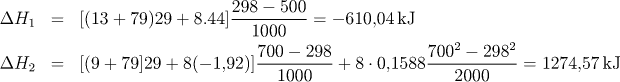
a celková změna je tedy
![]()
c) Bilance entalpie má v tomto případě tvar
![]()
Teplo ΔH2 má stejnou hodnotu, jako u bodu b). Pro teplo ΔH1 tedy platí
![]()
Tepelná kapacita výchozích látek je dána vztahem
![]()
Teplotu vstupních látek potom vypočítáme ze vztah
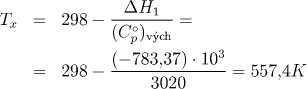
d) Bilance entalpie má v tomto případě tvar
![]()
Teplo ΔH1 je stejné, jako v bodě b). Pro tepelnou kapacitu produktů platí
![]()
Po dosazení číselných hodnot do bilance entalpie dostaneme
![]()
Po úpravě získáme kvadratickou rovnici
![]()
která má řešení
![]()
Druhý kořen rovnice je záporný a nemá fyzikální význam.