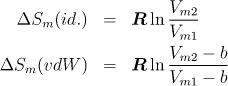4.4.2 Isobarická změna entropie s objemem pro ideální plyn a van der Waalsovu rovnici
Vypočtěte změnu entropie jednoho molu čistého plynu při izotermní
expanzi za teploty 300 K z objemu 200 cm3 na objem 15 dm3.
Předpokládejte platnost stavové rovnice:
a) ideálního plynu,
b) van der Waalsovy (a = 0,55 . 106 MPa . cm6 . mol−2, b = 64 cm3 mol−1).
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓