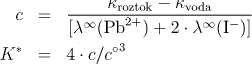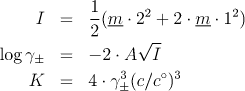7.1.16 Výpočet součinu rozpustnosti z konduktivity
Nasycený roztoku jodidu olovnatého má při teplotě 25 °C konduktivitu 3,82.10−2 S m−1, konduktivita použité vody je 1,8.10−4 S m−1. Limitní molární vodivosti mají hodnoty
![]()
Výpočet proveďte jednak za předpokladu ideálního roztoku a jednak s odhadem aktivitních koeficientů pomocí Debyeova-Hückelova zákona. Konstanta A Debyeova-Hückelova zákona má (pro dekadický logaritmus) hodnotu 0,509 mol−1/2kg1/2.
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓
↓