5.5 Chemický potenciál, aktivita, aktivitní koeficient v kapalné či tuhé fázi
Chemický potenciál i−té látky v kondenzované (kapalné či tuhé) fázi platí
![]()
kde μi•(T, p) = Gm,i•(T, p) je chemický potenciál (molární Gibbsova energie) čisté i−té složky za teploty a tlaku systému a ve stejné fázi jako je směs. Aktivitní koeficient γi je vyjádřen vztahem

V případě binárního systému je nejjednodušším vztahem pro dodatkovou Gibbsovu energii empirický vztah (tzv. regulární roztok)
![]()
V tomto případě pro aktivitní koeficienty dostaneme rovnice
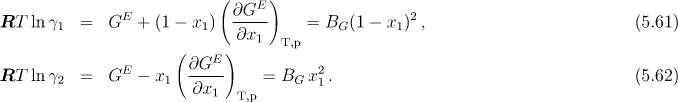
![]()
kde γ1∞, γ2∞ se označují jako limitní aktivitní koeficienty.
Volíme-li standardní stav čistá složka za teploty a tlaku soustavy (a stejné fáze jako má směs), dostaneme pro aktivitu látky (ze vztahu (5.50) a (5.58))
![]()
![]()
Aktivitní koeficienty nejsou nezávisle proměnné, ale platí mezi nimi vztah tzv. Gibbsova-Duhemova rovnice (uvažována binární směs - srovnej s (5.26) )
![]()
V případě omezeně rozpustných či mísitelných látek se používá pro rozpuštěné látky standardní stav ,,nekonečného zředění" a pro chemické potenciály platí (indexem 1 budeme označovat rozpouštědlo a indexem 2 rozpuštěnou látku)

kde μ2[x] resp. μ2[c] resp. μ2[m] je
chemický potenciál druhé složky získaný extrapolací z nekonečného zředění
na x2 = 1 resp. c2 = c2° resp. m2 = m2°. Standardní koncentrace
c2° resp. molality m2° mají obvykle hodnoty
c2° = 1 mol/dm3 resp. m2° = 1 mol/kg.
γ2[x], γ2[c], γ2[m] jsou aktivitní
koeficienty, které nabývají jednotkové hodnoty při
nekonečném zředění
(x2 ⟶ 0, resp. c2 ⟶ 0 resp.
m2 ⟶ 0).
Při volbě standardního stavu ,,nekonečného zředění" je aktivita rozpuštěné složky vyjádřena některým z následujících vztahů
![]()
Pokud uvažujeme ideální chování, anebo je koncentrace rozpuštěné látky dostatečně nízká, je aktivita této látky dána relacemi
![]()
Pro závislost aktivitních koeficientů na teplotě a tlaku je možné ze vztahu (5.64) získat
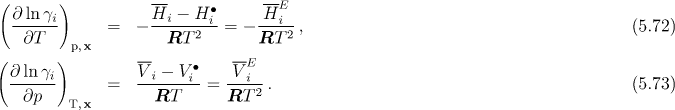
Příklady:
5.5.1 * Výpočet chemického potenciálu, aktivity a aktivitního koeficientu ze závislosti dodatkové Gibbsovy energie na složení (5.5.2 Výpočet dodatkové Gibbsovy energie ze znalosti aktivitních koeficientů (
5.5.3 Výpočet HE a γi ze závislosti GE = GE(T, x1) (
5.5.4 Diferenciální směšovací entalpie z GE = GE(T,x1) (